【摘要】目的探讨不同化疗方案治疗华氏巨球蛋白血症(WM)的临床疗效。方法将15例WM患者随机分为利妥昔单抗联合环磷酰胺为基础的化疗组(A组,8例)和氟达拉滨为基础的化疗组(B组,7例),比较两组化疗疗效和生存时间。结果A组治疗后完全缓解(CR)1例,部分缓解(PR)5例,微小缓解(MR)1例,疾病稳定(SD)1例;B组治疗后CR2例,PR3例,MR1例,SD1例。随访期间,A组患者生存率高于B组(100%vs.28.6%)(P<0.05)。结论利妥昔单抗联合环磷酰胺为基础的化疗方案在WM中的治疗效果优于氟达拉滨为基础的化疗方案。
【关键词】华氏巨球蛋白血症;利妥昔单抗;环磷酰胺;氟达拉滨
华氏巨球蛋白血症(WM)是成熟B淋巴细胞增殖性疾病,属于罕见的B淋巴细胞恶性肿瘤,其特点是骨髓中出现浆细胞样淋巴细胞浸润,伴血清单克隆IgM增高。WM患者的生存差异较大[1],一般生存期为5~10年[2]。根据WM的国际预后评分系统(IPSSWM)将其分为低危、中危和高危组,危险因素包括年龄>65岁、血红蛋白≤115g/L、血小板≤100×109/L、β2微球蛋白>3mg/L、IgM>70g/L。其中,低危组≤1个危险因素(年龄除外),中危组2个危险因素或者年龄>65岁,高危组>2个危险因素,三组5年生存率分别为87%、68%、36%[2]。在第3届国际WM研讨会中,工作组认为延长剂量的利妥昔单抗联合化疗至少能与单用核苷类似物、烷化剂、标准剂量的利妥昔单抗产生同样的治疗效果[3]。本文回顾性分析我院15例WM患者应用利妥昔单抗联合化疗或单用化疗的疗效,现将结果报道如下。
资料与方法
一、一般资料
2002年4月—2014年6月收集15例WM患者的临床资料,根据治疗方法的不同,将其分为利妥昔单抗联合环磷酰胺为基础的化疗组(A组,8例)和氟达拉滨为基础的化疗组(B组,7例),两组在年龄、性别构成比、IPSSWM分组等指标比较无统计学差异(表1)。WM诊断标准[4]:(1)存在不同程度血清单克隆IgM增高(无需考虑血清IgM具体的增高水平);(2)小淋巴细胞、浆细胞样淋巴细胞和浆细胞以小梁间浸润模式浸润骨髓;(3)免疫表型:CD19+,CD20+,CD5+/-,CD10-,CD23-,IgM+。
表1 两组患者基本临床资料(例)
| 项目 | A 组(n=8) | B组(n=7) | P 值 |
| 年龄 | 0.282 | ||
| >65岁 | 1 | 3 | |
| ≤65岁 | 7 | 4 | |
| 性别 | 1.000 | ||
| 男 | 6 | 5 | |
| 女 | 2 | 2 | |
| 血红蛋白 | 1.000 | ||
| ≤115g/L | 6 | 6 | |
| >115g/L | 2 | 11 | |
| 血小板 | 0.608 | ||
| ≤100×109/L | 2 | 3 | |
| >100×109/L | 6 | 4 | |
| β2微球蛋白 | |||
| ≤3mg/L | 1 | 4 | 0.119 |
| >3mg/L | 7 | 3 | |
| IPSSWM | 0.935 | ||
| 低危 | 3 | 2 | |
| 中危 | 3 | 3 | |
| 高危 | 2 | 2 |
二、方法
1.疗效评价[3] 根据第3届国际 WM 研讨会 专家共 识,完 全 缓 解(CR):血清 单 克 隆IgM 消 失, 骨髓中无浆细胞样淋巴细胞浸润,CT 扫描 示 淋 巴 结或器官肿大消失,无 WM 相关的症状。部分缓解 (PR):血清单克隆IgM 水平下降至少超过50%,临 床体检或 CT 示淋巴结 或 器 官 肿 大 至 少 缩 小 一 半, 无疾病相 关 的 新 症 状 出 现。微 小 缓 解(MR):血清 单克隆IgM 水平下降至少达25%但不超过50%,无 疾病相关的新症状出现。疾病稳定(SD):血清单克 隆IgM 水平下降少于25%,并且IgM 水 平 增 高 也 小 于 25%,无 疾 病 相 关 的 症 状 进 展。 疾 病 进 展 (PD):血清单克隆IgM 水平增加至少达25%,疾病 相关的有意义症状或者体征进展(例如贫血、血小板 减少、白细胞减少、器官肿大、WM 相关症状)。
2.治疗方法 A 组采用利妥昔单抗联合环磷 酰胺为基础的化疗(利妥昔单抗375mg·m-2·d-1 第1天,环 磷 酰 胺 750mg·m-2 ·d-1静 脉 注 射 第 2天,长 春 地 辛3mg·m-2·d-1静脉注射第2天,地 塞米松15mg静脉注射第2~6天),7例患者为初治,1例患者既往使用沙利度胺和苯丁酸氮芥治疗后疾病处于PD。B组采用单药氟达拉滨方案化疗(氟达
拉滨30mg·m-2·d-1静脉注射第1~5天)4例,氟达拉滨联合环磷酰胺方案(氟达拉滨30mg·m-2·d-1静脉注射第1~3天,环磷酰胺300mg·m-2·d-1静脉注射第1~3天)3例;6例 患 者 为 初 治,1例 患 者经 COP方案(环磷酰胺750mg·m-2·d-1静脉注射第1天,长春地辛3mg·m-2·d-1静脉注射第1天,地塞米松15mg静脉注射第1~5天)化疗后疾病处于SD。
三、统计学处理
采用SPSS17.0软件进行统计学分析,计数资料用 百 分 比 表 示,行 卡 方 检 验,Kaplan-Meier 和Log-rank分别描绘和检验生存曲线。P<0.05为差异有统计学意义。
结 果
一、治疗反应
A组治疗后CR1例,PR5例,MR1例,SD1例;B组治疗后 CR2例,PR3例,MR1例,SD1例;两组疗效相似。
二、不良反应
A 组患者的化 疗 耐 受 性 良 好,3例 发 生Ⅲ度 中性粒细胞减少,未发生严重感染等不良事件。B 组患者对化疗耐受相对较差,治疗过程中2例合并肺部感染,1例合并胃肠道感染,1例合并肺部感染和脑内脱髓鞘病变。
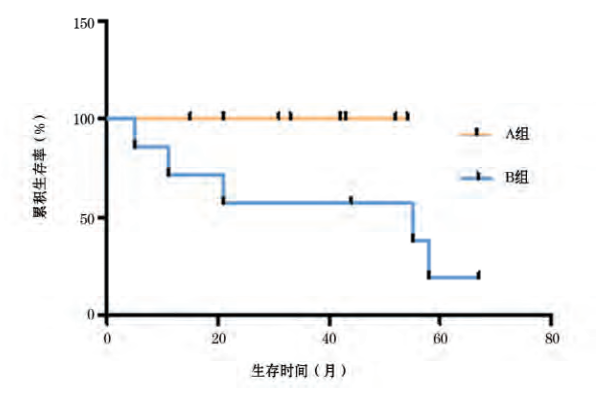
图1 患者生存分析
三、生存分析
A 组8例患者随访时间为15~54个月,中位随访时间为37.5个月,均 存 活;B 组7例患者随访时间为5~78个月,中位随访时间为44.0个月,中位生存时间为55.0个月,1例因突发 心 肌 梗 死 死 亡,1例因合并肺部侵袭性真菌感染及脑内脱髓鞘病变死亡,1例因 合 并 肺 部 细 菌 感 染 死 亡,2例 因 PD死亡,2 例 存 活;A 组 生 存 率 高 于 B 组 (100% vs.28.6%)(P<0.05)(图1)。
讨论
本文主要探讨两种不同化疗方案治疗 WM 的缓解率及患者生存情况,发 现 A 组 和 B 组 疗 效 相似,A 组生存率高于 B组。第4届国际 WM 工作组共识,一线治疗包括利妥昔单抗联合核苷类似物及环磷酰胺、利妥昔单抗联合核苷类似物、利妥昔单抗联合环磷酰胺为基础的治疗(利妥昔单抗联合环磷酰胺、多柔比星、长 春 新 碱、泼 尼 松,或 者 利 妥 昔 单抗联合环磷酰胺 和 地 塞 米 松)、利妥 昔 单 抗 联 合 沙利度胺。利妥昔单抗是 人-鼠嵌 合 性 抗 CD20单克隆抗体,CD20几乎表达于所 有 正 常 和 恶 性 B淋 巴细胞,却 不 表 达 于 干 细 胞。利妥昔单抗通过抗体依赖性的细胞杀伤 作 用 和 补 体 依 赖 性 的 细 胞 杀 伤作用引起肿瘤细胞溶解。利妥昔单抗与CD20的结合还可诱导 肿 瘤 细 胞 凋 亡,并具有化疗增敏作用。Dimopoulos等[3]采用 DRC 方案(地 塞 米 松 20mg静脉注射第1~5天,利妥昔单抗375mg·m-2·d-1静脉注射第1天,环磷酰胺100mg·m-2·d-1口服第1~5天,每 天 2 次)治 疗 72 例 WM 初治 患 者,7%患者达到 CR,67%患者 达 到 PR,2年无 进 展 生存率为90%。Abonour等[5]报道 采 用 R-CHOP方案(利妥昔单抗375mg·m-2·d-1静脉注射第1天,环磷酰胺750mg·m-2·d-1静脉注射第2天,阿霉素60mg·m-2·d-1静脉注射第2天,长春地辛3mg·m-2·d-1静脉注射第2天,地塞米松15mg静脉注射第2~6 天)治 疗 的 16 例 初 治 WM 患 者,PR 率 为91%。氟达拉滨是一种氟化嘌呤核苷类似物,对淋巴细胞具有选择性,广泛应用于慢性淋巴细胞白血病、非霍奇金淋巴 瘤 等 多 种 血 液 系 统 疾 病 的 治 疗。目前,相继有多 个 应 用 氟 达 拉 滨 治 疗 WM 的报 道,例如在美国西 南 肿 瘤 协 作 组 中,182例患 者 采 用 单药氟达拉滨 的 化 疗,根 据 血 清 β2 微球 蛋 白 及IgM水平,将 其 分 为 低 危、中 危、高 危 组,总 缓 解 率 为36% ,低危、中 危、高 危 组 的 5 年总生存率依次为70%、51%、20%[6]。本文随访中,两组化疗后疗 效相似,但是生存时间有统计学差异,且 B 组 严 重 并发症的发生率较高。有报道,包含核苷类似物的化疗能够增加 Richters综合征、骨髓增生异常综合征或者继发性急性髓细胞的发生率[3]。在 美 国 西 南肿瘤协作组中,175例患者使用氟达拉滨化疗,其中7例死于治疗相关的并发症[6]。因氟达拉滨会引起严重的不良反应,且 WM 呈低度恶性[7],为避 免 治疗相关不良反应,我们建议慎用骨髓抑制较深的氟达拉滨为基础的化疗,而利妥昔单抗联合环磷酰胺为基础的化疗无干细胞毒性,骨髓抑制程度低,感染发生概率较低,对 于 WM 患者 是 积 极、有效的治疗方案。
参考文献
[1] Dhodapkar MV,Hoering A,Gertz MA,etal.Long-term survivalinWaldenstrom macroglobulinemia:10-yearfollow-up ofSouthwestOncologyGroup-directedintergrouptrialS9003[J].Blood,2009,113(4):793-796.
[2] DimopoulosMA,KastritisE,DelimpassiS,etal.TheInterna-tionalPrognosticScoringSystem for Waldenstrms macro-globulinemiaisapplicableinpatientstreatedwithrituximab-basedregimens[J].Haematologica,2008,93(9):1420-1422.
[3] Dimopoulos MA,Gertz MA,KastritisE,etal.Updateontreatmentrecommendations from the Fourth InternationalWorkshopon Waldenstrms Macroglobulinemia[J].J ClinOncol,2009,27(1):120-126.
[4] LouwVJ,WebbMJ.PrognosisandtreatmentofWaldenstrmsmacroglobulinemia[J].TransfusApherSci,2010,42(2):193-197.
[5] AbonourR,ZhangLA,RajkumarV,etal.PhaseⅡ pilotstudyof rituximab+CHOP in patients with newly diagnosedWaldenstrms macroglobuliemia,an Eastern CooperativeOncologyGroupTrial(StudyE1A02)[J].Blood,2007,110:3616(abstr).
[6] Dhodapkar MV,JacobsonJL,Gertz MA,etal.Prognosticfactorsandresponsetofludarabinetherapyinpatients withWaldenstrm macroglobulinemia:results of United Statesintergrouptrial(SouthwestOncologyGroupS9003)[J].Blood,2001,98(1):41-48.
[7] KastritisE,KyrtsonisMC,HadjiharissiE,etal.Validationofthe International Prognostic Scoring System (IPSS)forWaldenstrmsmacroglobulinemia(WM)andtheimportanceofserumlactatedehydrogenase(LDH)[J].Leuk Res,2010,34(10):1340-1343.
由于网页排版的限制,导致部分内容可能产生歧义,请点击下方下载按钮下载论文原文PDF版。